
白蛋白紫杉醇的过去
上世纪60年代,美国科学家在太平洋紫杉树的树皮中发现了抗癌活性成分——紫杉醇。没多久,紫杉醇就被提取纯化和试验,于1992年获批用于卵巢癌治疗。
然而单靠从紫杉树中提取获得紫杉醇远不足以满足临床众多患者的需求,科学家们就继续开展研究,并从欧洲紫杉中发现了丰富的半成品,用它来半合成紫杉醇,解决了紫杉醇的供应问题。
然而,紫杉醇只有依靠聚氧乙烯蓖麻油溶解才能保证一定的溶解性和稳定性,但在20%~40%的患者中,注射该溶剂会导致严重的过敏反应。为了预防和减少过敏,患者在治疗前需要预先使用激素药物,同时紫杉醇在静脉注射之前需要大量稀释,因此完成一次紫杉醇注射,一般需要3小时,甚至更久。针对紫杉醇不易溶于水的特性,科学家又经过了十多年的研究,利用白蛋白作为纳米载体来承载紫杉醇。白蛋白是人体自身的蛋白,不会像蓖麻油那样引发免疫反应。

应用白蛋白纳米技术制备的白蛋白结合型紫杉醇(以下简称:白蛋白紫杉醇),不仅解决了过敏问题,还提高了治疗效果。在对乳腺癌的治疗中,常规的紫杉醇治疗只能达19%的缓解率,而白蛋白紫杉醇可以提高到33%[1]。在中国进行的晚期乳腺癌一线治疗的临床试验中(CA201),白蛋白紫杉醇治疗后的客观缓解率达到了56%,而对照组使用常规化疗药物只能达到27%[2]。此外,白蛋白紫杉醇也大大降低了对中性粒细胞的毒性,治疗后严重中性粒细胞减少事件只有紫杉醇的一半,同时也大大缩短了注射所需时间,半小时即可完成注射[1]。白蛋白紫杉醇的药效之所以能够提高,是因为纳米载体能够将药物快速传递到癌组织,且停留时间更长。

因为科学家的不断深入研究和纳米技术的发展,使得一个天然化合物的抗癌药用价值得到了大大提高,进化成为一个副作用更小、治疗效果也更好的药物。
白蛋白紫杉醇的今天
在美国,白蛋白紫杉醇已被用来正式治疗乳腺癌、非小细胞肺癌、胰腺癌等。2009年,白蛋白紫杉醇正式进入中国市场,但目前正式批准的适应症尚只有乳腺癌。2018年,在中国CSCO乳腺癌治疗指南中,白蛋白紫杉醇被推荐用于既往蒽环类治疗失败的患者,推荐级别为1A级。随着中国对癌症药物批准政策的改变,新的适应症批准也将加速,将会有越来越多的患者或可获益于白蛋白紫杉醇。
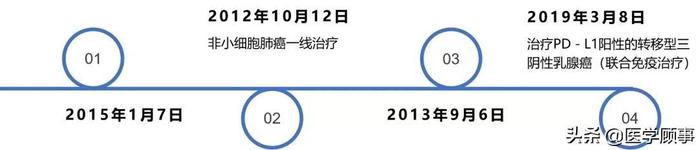 美国FDA关于白蛋白紫杉醇的批准历史
美国FDA关于白蛋白紫杉醇的批准历史中国每年因为乳腺癌、肺癌、胰腺癌去世的患者约64万人,占所有癌症死亡数的22%[3],近年来公布的白蛋白紫杉醇在这些癌种中的临床试验结果给这些肿瘤患者带来了希望。在肺癌临床试验中,白蛋白紫杉醇与紫杉醇相比,对鳞状细胞癌(41% vs 24%)和大细胞癌(33% vs 15%)的客观缓解率更高[4]。此外,白蛋白紫杉醇和紫杉醇分别联合卡铂进行治疗,白蛋白紫杉醇组的中位数无进展生存期为10.9个月,比紫杉醇组的4.9个月提高了一倍,白蛋白紫杉醇组的中位数总生存期为17.5个月,也比紫杉醇组的11.1个月增加了半年。对于晚期胰腺癌,吉西他滨化疗后两年的生存率只有4%,而白蛋白紫杉醇联合化疗把生存率翻了一番,提高到了9%[5]。
白蛋白紫杉醇的未来
免疫治疗是目前最火的癌症治疗方法,目前美国有7款免疫治疗的抗体药物获批用于各种癌症治疗,中国也有抗体药获得批准。然而,免疫治疗也有一定的局限,比如肺癌因为基因突变比较多,肿瘤组织里免疫细胞也比较多,是比较适合免疫治疗的“热肿瘤”,但是如果晚期患者PD-L1表达量不高,也需要联合化疗才能在一线治疗中显示出治疗效果。
三阴性乳腺癌一直以来的药物治疗主要是依靠化疗,一但耐药就束手无策。研究者对三阴性乳腺癌的一个新的治疗思路是免疫治疗联合化疗,通过化疗杀伤癌细胞,把“冷肿瘤”改变成“热肿瘤”,从而提高免疫治疗的效果。但不是任何一个化疗药物都可以用来联合免疫治疗的,比如紫杉醇因为需要使用类固醇激素来防止过敏反应,因此会大大降低免疫治疗的疗效,而白蛋白紫杉醇不存在类固醇的问题,且能在癌组织中快速富集,因此成为与免疫治疗强强联合的首选。
在早期临床试验中,抗PD-L1抗体Atezolizumab与白蛋白紫杉醇联用在转移性三阴乳腺癌的一线治疗中取得了53.8%的客观缓解率[6]。在PD-L1阳性患者中的三期临床试验结果表明白蛋白紫杉醇联合PD-L1抗体治疗获得了25个月的总生存期,明显高于白蛋白紫杉醇单独治疗(15.5个月)[7]。
但是白蛋白紫杉醇的联合治疗并不只局限于PD-L1抗体,目前有联合PD-1抗体的临床试验正在进行,包括一个对三阴乳腺癌的三期临床。白蛋白紫杉醇的联合免疫治疗也不局限于三阴乳腺癌,根据文献报道,有两例HER2阳性的乳腺癌患者在使用各种HER2靶向治疗药物之后产生耐药性,但是在白蛋白紫杉醇联合PD-1抗体治疗后获得了缓解[8]!借力于白蛋白紫杉醇,乳腺癌的治疗终于走进了免疫治疗时代。

2018年ESMO大会上报道的Atezolizumab 联合白蛋白紫杉醇对转移型三阴性乳腺癌治疗效果
参考文献:
1. Gradishar, W.J., et al., Phase III trial of nanoparticlealbumin-bound paclitaxel compared with polyethylated castor oil-basedpaclitaxel in women with breast cancer. J Clin Oncol, 2005. 23(31): p. 7794-803.
2. 姜晗昉, et al., 白蛋白结合型紫杉醇治疗晚期乳腺癌的临床观察. 2013.
3. Chen,W., et al., Cancer statistics in China,2015. CA Cancer J Clin, 2016. 66(2):p. 115-32.
4. Socinski,M.A., et al., Weekly nab-paclitaxel incombination with carboplatin versus solvent-based paclitaxel plus carboplatinas first-line therapy in patients with advanced non-small-cell lung cancer:final results of a phase III trial. J Clin Oncol, 2012. 30(17): p. 2055-62.
5. VonHoff, D.D., et al., Increased survival inpancreatic cancer with nab-paclitaxel plus gemcitabine. N Engl J Med, 2013.369(18): p. 1691-703.
6. Adams,S., et al., Atezolizumab Plusnab-Paclitaxel in the Treatment of Metastatic Triple-Negative Breast CancerWith 2-Year Survival Follow-up: A Phase 1b Clinical Trial. JAMA Oncol,2018.
7. Schmid,P., et al., LBA1_PRIMpassion130: Resultsfrom a global, randomised, double-blind, phase III study of atezolizumab (atezo)+ nab-paclitaxel (nab-P) vs placebo + nab-P in treatment-naive, locallyadvanced or metastatic triple-negative breast cancer (mTNBC). Annals ofOncology, 2018. 29(suppl_8).
8. Li, B.,et al., Remarkable response withpembrolizumab plus albumin-bound paclitaxel in 2 cases of HER2-positivemetastatic breast cancer who have failed to multi-anti-HER2 targeted therapy.Cancer Biology & Therapy, 2018. 19(4):p. 292-295.











