近日,FDA宣布,授予新型候选药物HIF-2α抑制剂MK-6482"突破性疗法"认定,用于治疗林岛(Von Hippel-Lindau,VHL)综合征相关的肾细胞癌患者。
这些患者携带的非转移性肾癌肿瘤大小小于3厘米。此前,FDA还授予MK-6482“孤儿药”资格。
◎ VHL相关肾细
VHL病是一种罕见的遗传病,全球患者约20万名。VHL病患者有发生良性血管肿瘤以及包括肾癌在内的多种癌症的风险。高达60%的VHL疾病患者会发展为肾细胞癌,这也是VHL患者死亡的主要原因。
肾细胞癌是最常见的肾癌,10个肾癌患者中大约9个是肾细胞癌,而10个肾细胞癌中大约有7个是透明细胞。据估计,2018年全球约有40.3万肾癌确诊病例,约17.5万人死于肾癌。
而透明细胞肾细胞癌(ccRCC)是肾细胞癌中最常见的类型,约占所有肾细胞癌的80%以上,是一种以恶性上皮细胞为特征的肿瘤,具有清晰的细胞质和紧密的巢状生长模式,并伴有复杂的树状血管。
ccRCC患者在早期无明显症状,多数患者在确诊时病情已发生转移,预后较差。
◎ 创新药MK-6482
在大多数透明细胞肾癌(约90%)患者中,当肿瘤抑制蛋白VHL失活时,缺氧诱导因子(HIF)蛋白在癌细胞内积累,发出缺氧这一错误信号,激活血管的形成,刺激了肿瘤的生长。
而MK-6482(原名:PT2977)是一种创新、强效、选择性的口服HIF-2α抑制剂,靶向缺氧诱导因子(HIF)-2a,可以阻断细胞的生长、增殖以及阻止异常血管形成。
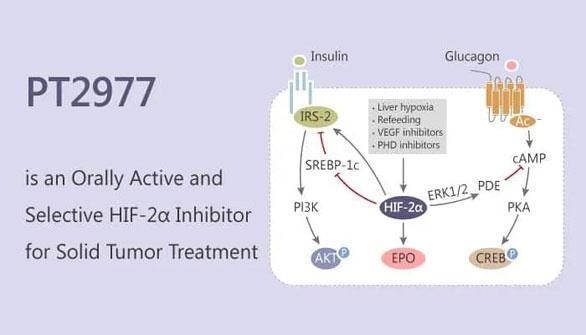
目前,MK-6482的多项临床试验正在进行中,包括晚期肾细胞癌、VHL相关性肾细胞癌以及晚期实体瘤患者。
◎ 两项临床试验
这项资格认定的授予是基于一项I/II期临床试验(NCT02974738)的结果,研究纳入了55例晚期透明细胞肾细胞癌患者。该试验数据已在2020年美国临床肿瘤学会年会上发表。
结果显示,中位随访13个月后,患者的总缓解率(ORR,n=13/55)为24%,41例患者病情稳定,而完全缓解+部分缓解+病情稳定的疾病控制率为80%。且该药的耐受性和安全性良好。
其中,5名高风险患者中有2名出现了部分缓解,40名中风险患者中有10名出现了缓解,10名低风险患者中有1例。
MK-6482在VHL相关的初治ccRCC患者中显示出良好的的抗肿瘤活性和耐受性。
目前,VHL疾病相关的肾细胞癌患者临床治疗选择仍然有限,期待新型抗癌药物MK-6482尽早获批,无论是在低、中、高风险还是在严重难治人群中,都能为患者带来良好的临床获益。











