机器之心报道
参与:张倩、蛋酱
昨晚,针对网上流传的抗病毒药物瑞德西韦在武汉「显效」的传闻,负责该药物临床试验的中日友好医院副院长曹彬教授已公开表示,这一说法不实。尽管我们对瑞德西韦抱有「比较高的期望」,但三期临床试验才刚刚开始,试验结果仍需等待。从试验的注册信息我们可以知道一些相关细节。

2 月 6 日晚,曹彬回复中国青年报记者,瑞德西韦在短期内治疗新冠肺炎效果显著的相关传闻为不实信息。
1 月 31 日,《新英格兰医学杂志》所刊发的论文中提及美国首例新冠肺炎患者接受了瑞德西韦静脉注射(因病情危急,医生采取「同情用药」),一天后症状得到极大缓解。
这一案例引发了极大关注。尽管并不能判定该患者症状缓解与瑞德西韦直接相关,但确实促使瑞德西韦以非常快的速度进入了针对新型冠状病毒的三期临床试验阶段。
在临床试验所用的瑞德西韦运抵中国以后,2 月 5 日下午,中日友好医院王辰、曹彬团队在武汉市金银潭医院宣布启动瑞德西韦治疗新型冠状病毒感染的临床研究,研究有两项:
- 一项研究评估瑞德西韦用于确诊感染 2019-nCoV 且已住院但未表现出显著临床症状(如,需要额外吸氧)的患者的治疗效果;
- 一项研究则评估瑞德西韦用于出现较严重临床症状(如,需要吸氧)的确诊病患的疗效。
761 位病例已顺利入组,包括轻、中症患者 308 例,重症患者 453 例。
在 2 月 6 日首批患者接受用药的报道出现之后,互联网上出现了「瑞德西韦短时间内已在 761 位患者身上全部显效」一类的说法。对此,曹彬公开表示:「临床研究今天才开始,怎么可能知道结果?」
试验注册信息
在美国临床试验资料库 ClinicalTrials.gov中,两项瑞德西韦治疗新型冠状病毒肺炎临床试验的注册信息已经上线。ClinicalTrials.gov 是美国国立医学图书馆(NML)与美国食品与药物管理局(FDA)运行的临床试验资料库。其主旨是向医学研究人员和机构提供临床试验注册服务,同时为患者、医疗卫生人员和公众提供临床试验信息查询服务。
这两项注册信息分别涉及瑞德西韦的轻中症患者试验和重症患者试验,从中可以检索到两项临床试验的资助单位/项目负责人、给药方式、入组条件、试验终点应用指标等重要信息。
- 针对中/轻症状患者的临床试验注册信息「Mild/Moderate 2019-nCoV Remdesivir RCT」:https://clinicaltrials.gov/ct2/show/NCT04252664
- 针对重症患者的临床试验注册信息「Severe 2019-nCoV Remdesivir RCT」:https://clinicaltrials.gov/ct2/show/NCT04257656?cond=2019-nCoV&cntry=CN&draw=2&rank=1
针对中/轻症状患者的临床试验注册信息
中、轻症状患者临床试验的时间节点如图所示:2 月 5 日开始,4 月 27 日完成试验。

治疗给药方式为:试验组和对照组在第 1 天分别给予瑞德西韦和安慰剂 200 毫克负荷剂量,然后每天一次 100 毫克静脉内维持剂量,持续 9 天。
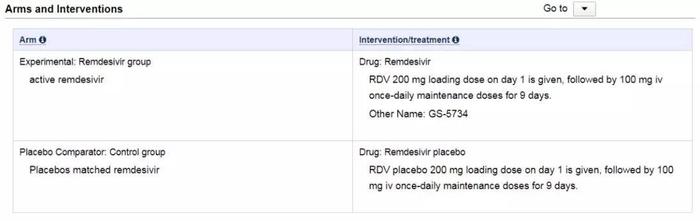
此前网上流传的说法中,「全部病例 48 小时内全部退烧」被视为鉴定药效的标准。但从试验注册信息来看,如果想要证实瑞德西韦对治疗新冠肺炎确实有效,这一指标是不够的。中/轻症患者试验注册信息指出,判断病人恢复正常的指标涉及体温、血氧饱和度、呼吸频率、咳嗽程度等。

在进组要求方面,注册信息显示,参与中/轻症试验的患者需要在 18 周岁以上,且发病不超过 8 天;患有严重肝病、肾损伤,处在哺乳期、孕期、已知对瑞德西韦有过敏反应或此前 30 天内参与过 2019-nCov 相关试验治疗的病人都不能参与此次试验。

参与轻、中症试验需要满足的条件。

不能参与轻、中症试验的人群。
针对重症患者的临床试验注册信息
重症患者试验注册信息与中、轻症患者信息略有差别,具体表现在试验完成时间、进组要求等方面。
信息显示,重症组的试验也已于 2 月 5 日开始,预计将于 5 月 1 日结束。

与轻、重症患者组相比,重症患者的入组标准略有差别,如要求发病时间不超过 12 天等。

参与重症试验需要满足的条件。
同时,「排除标准」从 8 条减少到 6 条,去掉了「已知对瑞德西韦有过敏反应」等条件。

不能参与重症试验的人群。
其他试验注册信息
当然,除了瑞德西韦,国内还有多项针对新型冠状病毒的试验正在进行。如果想了解更多试验的详细信息,大家可以登录「中国临床试验注册中心」网站查询:http://www.chictr.org.cn/searchproj.aspx。
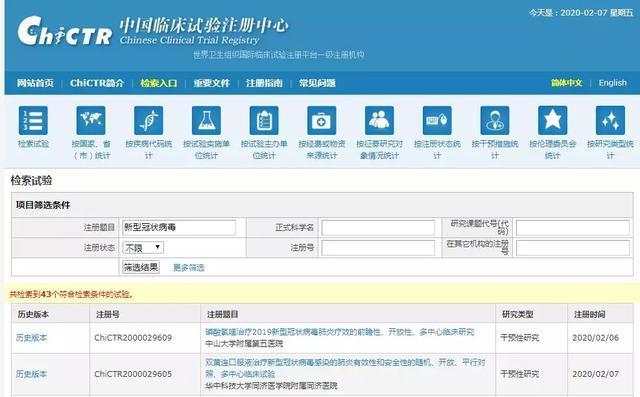
「中国临床试验注册中心」网站检索页面,磷酸氯喹、双黄连口服液等相关药物试验注册信息都可以在该网站查到。
我们和特效药之间的「距离」
距离疫情爆发已有一段时间,随着多项新型冠状病毒相关研究的展开,人们对新冠肺炎特效药研发的相关问题关注度很高。
在 2 月 5 日晚的《新闻 1+1》节目中,主持人白岩松曾就特效药问题咨询了中国工程院副院长、中国医学科学院院长王辰:「特效药什么时候出来?我们是否可以收获一点乐观的信息?」
王辰表示:「大家必须清楚,要想战胜疫情的话必须有两条工作主线,一条工作主线就是防控和医疗,另外一条主线就是科学研究。」
「根据前期的结果,我们对瑞德西韦抱有比较大的希望,其他药物包括中药,我们都需要进一步的临床观察来确定其疗效。特别提醒大家的是,个例的药品有效与否不是科学结论,一定要进行临床试验。」
钟南山院士也公开表示,临床试验可以加快绿色通道,但必须走程序。「很多试验室找到一个苗头,就希望马上完全进入临床,这个要小心,伦理审查一定要通过。」
目前,除了期盼度比较高的瑞德西韦,人们所知道的药物还有北京大学第一医院呼吸和危重症医学科主任王广发在自身治疗过程中所使用的抗艾滋病药物克力芝(洛匹那韦利托那韦片),以及李兰娟团队公布的阿比朵尔和达芦那韦,后两种药物可用于抑制冠状病毒。
但总体来说,尚未有研究证实某种药物能够针对新型冠状病毒肺炎患者产生「特效」。至于瑞德西韦的有效性,我们还要等待临床试验的进一步验证。
在这场抗疫战中,我们都期盼针对新冠肺炎的特效药尽快出现,早一分钟,或许就可以多挽救一个人的生命。
2 月 7 日凌晨,武汉中心医院官方微博发布消息表示,该院眼科医生李文亮因感染新型冠状病毒肺炎,经抢救无效,已于 2 月 7 日凌晨 2 点 58 分去世。
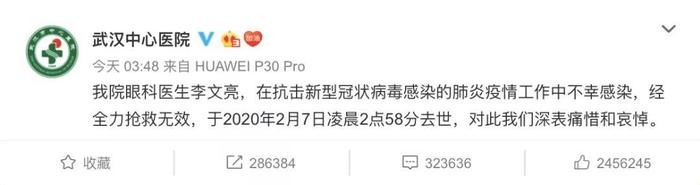
令人遗憾的是,李文亮医生未能等到特效药到来的一天。











