美国临床肿瘤学会(ASCO)年会是每年肿瘤学领域最重要的一次会议,囊括了大批创新疗法的最新临床进展,今年由于受新冠疫情影响,ASCO年会改为于5月29日-5月31日(美国东部时间)首次以线上形式举行,本次会议的主题为:团结征服、共同进步。近年来,在政策、资本、人才等多方因素共同促进下,众多中国创新药企脱颖而出,研究成果频频唱响世界舞台。
【肿瘤资讯】在追踪本次ASCO年会的同时,也特别关注到有关于国产原创新药的相关进展,其中令人瞩目的是,来自亚盛医药的3款细胞凋亡系列原创新药——MDM2-p53抑制剂(APG-115)、IAP抑制剂(APG-1387)和Bcl-2/Bcl-xL双靶点抑制剂(APG-1252)公布的四项最新数据,其涵盖了治疗晚期肉瘤和其他转移性实体瘤的初步结果。
由于这三款细胞凋亡药物涉及的靶点目前为止全球都还没有批准上市的药物,因此这三个创新小分子药都是有潜力成为全球同类第一或者是同类最佳的产品,即first in class 或 best in class,其四个摘要全部上榜presentations, 其中有三项研究入选poster discussions。为此,小编特根据药物作用的相关靶点及相关临床研究进行梳理与报道。
初探之光——I期结果亮相ASCO,原创新药潜力无穷
一、新靶点MDM2-p53 抑制剂类抗肿瘤药物
两项重要研究荟萃:
研究一:新型MDM2小分子抑制剂APG-115与帕博利珠单抗在美国联合治疗转移性实体瘤患者的Ib期研究
摘要编号:#3512
研究详情及主要结果:
该研究是一项在美国进行的开放、多中心的Ib /II期临床研究 ,旨在评估APG-115与帕博利珠单抗联合使用一般耐受性良好。最常见的药物相关性不良反应(TRAEs)(≥10%)包括:恶心、呕吐、疲劳、血小板计数减少、中性粒细胞计数减少、食欲下降、腹泻和甲状腺功能减退等。
疗效观察显示,在18例疗效可评估患者中,1例获得长达20个月的完全缓解(CR)(目前仍处于治疗中),2例获得长达8-9个月部分缓解(PR)(1例经纳武单抗治疗3个月失败的非小细胞肺癌患者,1例未经肿瘤免疫治疗的阑尾腺癌患者),以及7例达到1.5-7个月的疾病稳定(SD)。客观缓解率(ORR)为16.7%,疾病控制率(DCR)为55.5%。获得完全缓解的患者如下:
55岁白人女性, 2014 年诊断为stage IIIc卵巢浆液细胞癌,经过手术和含铂类辅助化疗后6个月内复发 (stage IV),其后再经Doxil,Topotecan + Bevacizumab,抗癌管家-康爱管家,我们一起抗癌,治愈癌症不是梦。以及XMT1536 (靶向NaPi2b的ADC )等多线抗肿瘤治疗,病情仍旧进展;该患者在接受APG-115(100毫克)与帕博利珠单抗联合治疗4个周期后获得PR,8个周期后获得CR,之后维持CR,目前处于第25个周期治疗中。该名患者具有恶性肿瘤家族史,血液遗传学测定显示P53野生型,ATM 家族突变。
PK分析显示,在50-200毫克剂量范围内,APG-115的AUC 和Cmax 随剂量增加而增加,APG-115与帕博利珠单抗联合使用并未影响APG-115的PK参数。PD分析显示血清MIC-1(TP53活化的生物标志物)呈现出与剂量正相关的趋势。

结论:Ib期安全有效的临床数据表明APG-115与帕博利珠单抗的联合使用的前景广阔。针对具有特定生物标志物的癌症患者的II期临床试验目前正在进行中。
大咖点评
美国NEXT Oncology内科肿瘤学家Anthony W. Tolcher博士表示:“参加该研究的患者大部分都是临床上复发难治的或者已经转移的肿瘤病人,一般都为标准治疗失败或者是临床上无药可医的最后线的晚期癌症病人。对于这样的晚期癌症病人能够看到肿瘤得到控制、缩小甚至是完全缓解,是非常令人振奋的。特别是有一例卵巢癌患者已经过包括靶向药物治疗在内的多线治疗均失败,而卵巢癌本身就是“cold tumor”,即是对于免疫治疗不敏感的癌症。该患者使用APG-115联合治疗方案获得CR,且至今为止已经用药生存了二十多个月,还在继续治疗并保持CR,说明该联合治疗的疗效和长期使用的安全性。”
研究二:MDM2-p53 抑制剂 APG-115 在中国晚期脂肪肉瘤和其他实体瘤患者中的 I期研究结果
摘要编号:#11542
研究详情及主要结果:
截至 2020 年 1 月 9 日,21 例符合条件的晚期实体瘤患者接受 3 个剂量水平(100 mg、150 mg 和 200 mg)的 APG-115 治疗。脂肪肉瘤占所有瘤种的2/3。21 例患者中大部分完成至少 2 个周期的 APG-115 治疗,1 例患者已完成 6 个周期APG-115治疗。
对 19 例患者(4 例患者仍在治疗中)进行疗效评估,其中脂肪肉瘤 13 例。在这些患者中,1 例PR,12 例SD;ORR为 5.3%,DCR为 68.4%。表达野生型 TP53脂肪肉瘤患者(n=9)ORR高达 11.1%,DCR为 77.8%。
常见治疗期间出现TRAEs 包括贫血以及白细胞和血小板计数降低。然而大多数 AE 为 1 级或 2 级 ,100 mg 剂量组不良事件的发生率很低。
目前的研究发现,APG-115在隔日给药一次,连续给药21天停药7天的给药方案下,总体安全性且耐受性良好,尤其在100mg剂量水平;APG-115的RP2D为100mg 隔日给药。结论:APG-115单药在脂肪肉瘤及表达TP53野生型肿瘤的患者中看到了临床疗效,这一结果也支持我们之前的发现,即在脂肪肉瘤及其他肿瘤中TP53野生型是APG-115的疗效预测生物标志物。
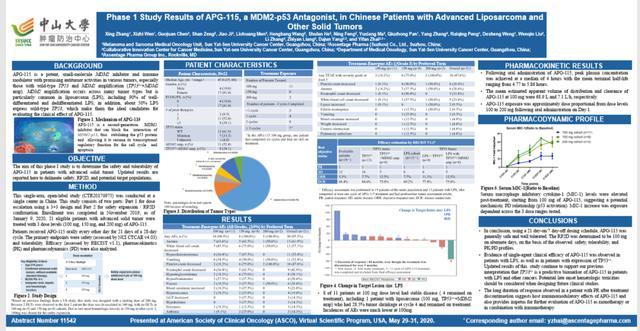
1 例 PR 患者停药后观察到的超过10个月的持续缓解,提示 APG-115可能具有宿主免疫调节作用,也为进一步评价 APG-115 单药治疗或与免疫治疗联合治疗提供了动力。
大咖点评
中山大学附属肿瘤医院黑色素瘤与肉瘤内科主任医师张星教授表示:“晚期脂肪肉瘤是恶性软组织肉瘤中常见的组织学类型,预后差、复发率高,现阶段缺乏有效的治疗方案。APG-115是高效的MDM2-p53抑制剂,去年ASCO的报道中在脂肪肉瘤方面的数据令人印象深刻。在更新的数据中,我们在100mg剂量组进行了安全性扩增,确定了其II期推荐剂量。同时进一步验证了之前的发现,TP53野生型是APG-115的疗效预测生物标志物,脂肪肉瘤可能是其潜在的目标瘤种之一。我们也期待更多临床研究及分子生物学证据。”
关于APG-115
APG-115是一种口服生物可利用的、高选择性的小分子MDM2抑制剂。APG-115对MDM2具有高度结合亲和力,通过阻断MDM2-p53相互作用从而恢复p53肿瘤抑制活性。目前,APG-115已在美国启动单药临床I期、联合帕博利珠单抗治疗晚期实体瘤/转移性黑色素瘤的临床 Ib/II试验、单药或联合化疗治疗唾液腺癌的I/II期等三项临床研究;作为首个在中国进入临床阶段的MDM2-p53抑制剂,APG-115在中国也获批开展包括单药I期研究、单药或联合化疗治疗AML/骨髓增生异常综合征(MDS)的Ib期研究等临床试验。
二、新靶点 IAP 抑制剂类抗肿瘤药物
研究介绍
新型双价IAP拮抗剂APG-1387联合帕博利珠单抗治疗晚期实体瘤的Ib期研究
摘要编号:#3508
研究详情及主要结果:
“新型IAP拮抗剂APG-1387与帕博利珠单抗联合治疗的Ib期研究显示,该联合治疗具有安全性,不良事件可控,这是支持APG-1387展开进一步研究的重要里程碑。此外,我们还观察到了一些令人激动的临床效果,这些现象值得我们在包括微卫星稳定型结直肠癌和非小细胞肺癌等特定的患者人群中展开进一步评估。特别值得关注的是,四例NSCLC患者均为对K药耐药或者是复发难治的病人,在联合治疗下肿瘤缩小达到PR,ORR达到50%,DCR达到100%(目前病例数比较少,试验进行中),充分显示初步疗效。”
截至2020年4月1日,在Ib期研究中,41例各种晚期实体瘤患接受了APG-1387和帕博利珠单抗的联合治疗,其中包括剂量递增部分的10例患者:20mg(n = 4),30mg(n = 3),45mg(n = 3);以及MTD剂量扩增部分的31名患者。剂量递增期间未观察到DLT,APG-1387的MTD确定为45mg。
APG-1387与帕博利珠单抗联合使用的耐受性良好,不良事件可控。最常见的TRAE(≥10%)是疲劳、头痛、恶心和斑丘疹。面神经障碍同样仅见于2名患者(4.9%),并没有高于单药研究。
在37例疗效可评估的患者中,有4例患者获得PR,其中2例NSCLC(非小细胞肺癌),1例CRC(结直肠癌)和1例BC(乳腺癌),以及12例患者获得SD。总体ORR为10.8%,DCR为43.2%。NSCLC队列达到了50%的ORR和100%的DCR;CRC队列获得1个PR和3个持久SD,达到了50%的DCR。
APG-1387的初步PK数据显示,在20-45 mg的剂量范围内,暴露(Cmax和AUC)与剂量成比例。
APG-1387的初步PD数据显示,APG-1387诱导了快速且显着的cIAP-1 / XIAP抑制作用,具有潜在的药效学作用。

结论:有效性和安全性数据表明,APG-1387与帕博利珠单抗联合使用是一种卓有潜力的抗肿瘤方法,在晚期NSCLC和CRC患者中值得进一步研究。
大咖点评
美国圣安东尼奥癌症治疗中心(The START Center for Cancer Care in San Antonio)临床研究副主任Drew W. Rasco博士表示:“新型IAP拮抗剂APG-1387与帕博利珠单抗联合治疗的Ib期研究显示,该联合治疗具有安全性,不良事件可控,这是支持APG-1387展开进一步研究的重要里程碑。此外,我们还观察到了一些令人激动的临床效果,这些现象值得我们在包括微卫星稳定型结直肠癌和非小细胞肺癌等特定的患者人群中展开进一步评估。特别值得关注的是,四例NSCLC患者均为对K药耐药或者是复发难治的病人,在联合治疗下肿瘤缩小达到PR,ORR达到50%,DCR达到100%(目前病例数比较少,试验进行中),充分显示初步疗效。”
关于APG-1387
APG-1387是一种新型小分子细胞凋亡蛋白抑制因子(IAP)抑制剂,主要用于用于治疗晚期实体瘤及慢性 HBV 感染。APG-1387 的主要优势在于其专为结合至 IAP 蛋白二聚体和单体而设。目前亚盛医药正在全球范围内开发APG-1387,且已在中国和澳大利亚完成针对实体瘤的临床I期剂量爬坡试验,正在美国进行与帕博利珠单抗联合治疗的Ib/II期临床试验。同时正在中国进行用于治疗乙型肝炎的Ib期临床试验,并于今年2月获批启动联合化疗治疗晚期胰腺癌的Ib/II期临床试验。
三、Bcl-2/Bcl-xL双重抑制剂- APG-1252
研究介绍
Bcl-2/Bcl-xL双靶点抑制剂palcitoclax (APG-1252)在美国转移性实体瘤患者中的首个人类试验显示,其在保持抗肿瘤效果的同时具有血小板安全性上的优势
摘要编号:#3509
研究详情及主要结果:
该研究旨在评价APG-1252 (palcitoclax)在美国转移性小细胞肺癌或其他恶性实体肿瘤的安全性/耐受性、药物动力学及初步的抗肿瘤活性。试验采取标准的“3+3”设计进行剂量递增。采取静脉给药(30分钟)每周两次或一次,28天为一周期。当MTD/ RP2D确定后,更多的患者将被纳入剂量扩增阶段。
截至2019年12月21日,共计42名患者分别参与了APG-1252 (palcitoclax) 10mg-400mg共8个剂量组的试验(31名患者在每周两次用药组,11名在每周一次用药组),剂量递增阶段已完成。
共观察到4例DLTs,均为4级血小板下降,发生于320mg及400mg。血小板减少是APG-1252(palcitoclax)的目标毒性反应,其计数在用药后快速下降并在2-6天之内未采取医疗干预的情况下迅速恢复正常。
在36例可评估疗效的患者中,共有3名分别患有小细胞肺癌、伴有低分化神经内分泌肿瘤的前列腺癌、高度恶性浆液性卵巢癌的患者取得了PR,其中小细胞肺癌患者的PR持续超过18个用药周期。另有7名患者达到SD的疗效,其中2名患者SD持续超过6周期,3名患者SD疗效维持4个周期以上。其余26名患者疾病进展,总体DCR为27.77%。
最常见副作用均为一级或二级。26.2%的患者有三级以上TRAEs。最常见TRAEs为血小板计数下降(14.3%),谷草转氨酶升高(9.5%)及谷丙转氨酶升高(7.1%)。
APG-1252(palcitoclax)在≤240mg的剂量中具有良好的耐受性。240mg每周一次用药被确定为MTD和RP2D。目前MTD的扩展试验进行中,已完成所有病人入组。
APG-1252(palcitoclax)在10-400mg剂量范围内呈现出线性药代动力学特征,且与剂量成正比。
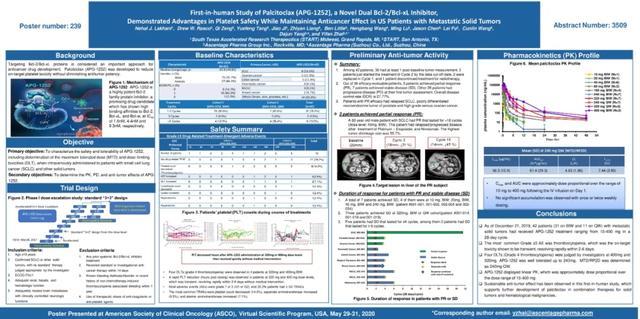
结论:APG-1252(Palcitoclax)的I期临床试验显示了可持续的抗肿瘤效应,此研究结果支持进一步开发联合APG-1252与其他治疗方法在恶性实体肿瘤及血液疾病的应用。
大咖点评
美国START Center for Cancer Care中西部癌症治疗中心(START Midwest)临床研究主任Nehal Lakhani 博士表示:“palcitoclax (APG-1252)是一个高效的新型Bcl-2家族蛋白抑制剂,诱导肿瘤细胞的凋亡。在美国开展的首次人类试验中,palcitoclax 显示了安全性、可耐受性以及早期的抗实体肿瘤效果。palcitoclax作为一个新型分子,也表现出了可预期的药物代谢特征。鉴于I期试验的安全性及有效性均表现良好,我们期待在某些特定种类的肿瘤疾病中进一步评估药物的抗肿瘤效果。”
关于APG-1252
APG-1252是一种Bcl-2/Bcl-xL双靶点抑制剂类药物,可通过选择性抑制Bcl-2及Bcl-xL蛋白恢复细胞凋亡,临床拟用小细胞肺癌(SCLC)、非小细胞肺癌(NSCLC)、淋巴癌等实体肿瘤的治疗。目前在美国、澳大利亚进行用于治疗晚期癌症患者的两项I期剂量递增试验,在中国进行作为单药治疗SCLC的一项I期剂量递增/扩展试验。
矢志创新——重启肿瘤细胞凋亡,原创新药未来可期
在肿瘤领域,安全有效的联合用药将是肿瘤治疗最重要的方向和主力,以期达到进一步提高靶向或是免疫治疗的疗效,并克服耐药,最终控制或者是治愈癌症。而我国的生物医药发展正处于高速发展及变革的阶段,国家层面出台众多的政策引导及促进提升医药产业水平,全球化与创新合作将成为未来的焦点,所以开拓创新、持续推进全球临床开发是医药企业的核心竞争力。
作为一家致力于肿瘤、乙肝及与衰老相关疾病等治疗领域开发创新药物的研发公司,亚盛医药(6855.HK)除了上述创新药以外,还有多种抗肿瘤药物进入临床研发阶段,其研发产品管线包括细胞凋亡路径关键蛋白的抑制剂、第二代和第三代癌症相关激酶突变体抑制等。据悉,目前已有8个1类新药进入临床开发阶段,正在全球开展I/II期临床试验30多项。同时,作为日益活跃在国际学术舞台的“中国声音”,亚盛医药已连续三年携多项原创新药临床进展亮相ASCO年会,并且获得了广泛的关注。
对于本次ASCO会议所公布的多项研究成果,亚盛医药董事长、CEO杨大俊博士表示:“此次在ASCO展示的多项数据体现了亚盛医药在细胞凋亡新药研发领域的全球临床开发的全面推进。抗癌管家-康爱管家,我们一起抗癌,治愈癌症不是梦。特别令人兴奋的是,MDM2-p53抑制剂APG-115、IAP抑制剂APG-1387的联合用药数据都显示了相当的潜力,值得进一步探索。未来将加快推进临床开发,期待早日为临床肿瘤患者提供更多治疗选择。”
本文转自抗癌管家网站-康爱管家











