
2021年6月17日,美国北卡大学Jeff Dangl实验室、中科院分子植物科学卓越创新中心万里研究组和美国杜克大学裴真明实验室合作在Science发表了题为“Plant ‘helper’ immune receptors are Ca
2+
-pe
rmeable non-selective cation channels
” 的研究长文,揭示了植物细胞内一类免疫受体作为钙离子通道调控免疫的分子机理。

研究背景
植物免疫系统识别病原微生物并激活免疫反应,限制病原菌侵染。NB-LRR(NLR)蛋白是植物细胞内主要的免疫受体,通过识别病原微生物效应蛋白引发免疫反应和细胞程序性死亡。植物的 NLR 根据其 N 端的信号转导结构域可以分为三类: TIR-NB-LRR(TNL)、 CC-NB-LRR(CNL)和CC
R
-NB-LRR(RNL)。TNL和CNL识别病原菌效应蛋白,RNL不直接识别病原菌效应蛋白,而是作用于 TNL 和 CNL下游,因此称为helper NLR(Jubic, et al. 2019)。RNL包含两类: NRG1和ADR1。在拟南芥中,NRG1作用于TNL下游介导细胞死亡的发生,而ADR1则作用于TNL下游介导抗性。2019年,中科院分子植物科学卓越创新中心万里研究员在博士后期间(Jeff Dangl lab)的研究表明,植物TNL识别病原菌被激活后作为NAD
+
降解酶并产生小的信号分子而引起细胞死亡(Wan, et al. 2019)。而NRG1/ADR1在TNL下游调控细胞死亡和抗性的分子机理未知。

图1 在人癌细胞中表达植物的helper NLR引起钙离子流入细胞
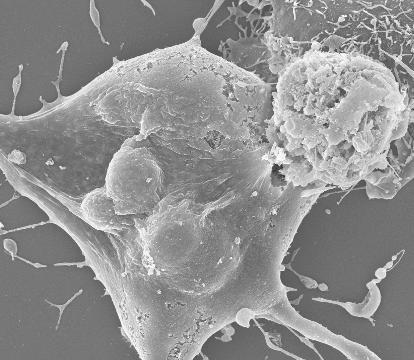
图2 在人癌细胞中表达植物的helper NLR引起细胞死亡
研究过程
本研究首先解析了拟南芥NRG1 CC
R
结构域的晶体结构,并发现CC
R
与动物中作为阳离子通道引发细胞坏死的MLKL在结构上有很大的相似性。进一步研究发现:在烟草和人癌细胞中表达NRG1的自激活突变体和野生型ADR1都能引起细胞死亡,且死亡表型依赖于质膜定位以及其介导的钙离子内流。电生理实验也证实了NRG1的自激活突变体是一个钙离子通透性但非选择性的阳离子通道。
所有拟南芥的TNL依赖下游的ADR1/NRG1介导免疫,因此本研究揭示了广泛TNL下游抗性和细胞死亡产生的分子机理。
2021年5月12日,中科院遗传与发育生物学研究所周俭民、陈宇航、何康敏和清华大学柴继杰合作在Cell发表研究论文证实ZAR1(CNL)抗病小体作为钙离子通道引发细胞死亡和免疫的分子机理(Bi, et al. 2021)。这两项研究成果综合阐明了CNL和TNL信号通路中相关NLR被激活作为钙离子通道引起抗性和细胞死亡的保守机制。

图3 植物TNL信号通路的工作模型
相关信息
美国北卡大学Jeff Dangl实验室的博士后Pierre Jacob和Nak Hyun Kim为该论文共同第一作者。美国北卡大学Jeff Dangl教授、中科院分子植物科学卓越创新中心万里研究员和美国杜克大学裴真明教授为该论文的共同通讯作者。该研究得到了中科院分子植物科学卓越创新中心人才启动经费,植物分子遗传国家重点实验室经费以及中科院先导专项经费的支持。
万里 研究员
植物病理学研究
2020年热文精选
1. 杯具了!满满一纸杯热咖啡中,满满的塑料微粒…
2. 美英澳科学家《自然医学》再添力证:新冠病毒乃自然进化产物,或有两种起源…
3. NEJM:间歇性禁食对健康、衰老和疾病的影响
4. 一年内治愈失眠!研究发现:改善睡眠,你或许只需要一条沉重的毯子
5. 哈佛新研究:仅12分钟的剧烈运动,能为健康带来巨大的代谢益处
6. 第一项人类干预试验:在大自然里“摸爬滚打”28天,足以提高免疫力
7. 垃圾食品是“真.垃圾”!它夺走了端粒长度,让人老得更快!
8. Cell解谜:不睡觉真的会死!但致死的变化不是发生在大脑,而是肠道…
9. 《自然通讯》超大规模研究:血液中铁的水平是健康与衰老的关键!
10. 不可思议!科学家一夜之间逆转动物“永久性”脑损伤,还让老年大脑恢复了年轻态…
来源:中国生物技术网











